AstraZeneca и японская компания Daiichi Sankyo сообщили о том, что Управление по контролю за продуктами и лекарствами США (FDA) приняло к рассмотрению их заявку на лицензирование нового биологического препарата (sBLA) для применения антитела-конъюгата Datroway (датопотамаб деруксикан) при лечении рака молочной железы. Данная заявка получила статус приоритетного рассмотрения.
Однако FDA также выдало полное ответное письмо (CRL) на заявку AstraZeneca на одобрение подкожной формы препарата Saphnelo (анифролумаб) для лечения взрослых пациентов с системной красной волчанкой. В настоящее время Saphnelo доступен на рынке в виде внутривенной инфузии и применяется для терапии умеренной и тяжелой форм SLE (системной красной волчанки).
Datroway: новый шаг в терапии рака молочной железы
Согласно информации, предоставленной AstraZeneca и Daiichi Sankyo, заявка на Datroway направлена на расширение его использования для лечения взрослых пациентов с неоперабельной или метастатической тройной отрицательной карциномой молочной железы (TNBC), которые не могут получать терапию с помощью ингибиторов PD-1/PD-L1. Эффективность Datroway уже была подтверждена глобальным исследованием третьей фазы TROPION-Breast02, в котором были продемонстрированы статистически значимые предпочтения в общей выживаемости по сравнению с химиотерапией.
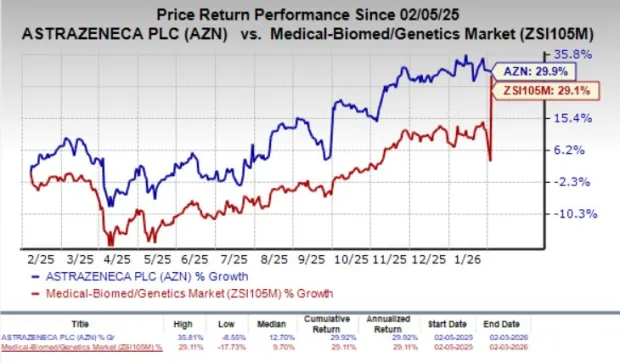
Фармацевтическая отрасль наблюдает рост интереса к препаратам, использующим антитела-конъюгаты, и Datroway стал значительным улучшением в этом направлении, особенно благодаря своей способности обеспечивать более высокий объективный ответ и продолжительность ответа по сравнению с химиотерапией. По сравнению с индексом акций в данной области (29,1%), акции AstraZeneca выросли на 29,9% за последний год, что свидетельствует о высоком спросе на новейшие медицинские решения.
На данный момент Datroway также одобрен в США по ускоренной программе для лечения взрослых пациентов с локально распространенным или метастатическим раком легкого с мутацией EGFR, которые не ответили на терапию, направленную против EGFR, и химиотерапию на основе платины. Препарат продолжает оцениваться в нескольких завершающих исследованиях на различных типах онкологических заболеваний, включая рак легкого, молочной железы и уротелиальный рак.
Сложности с Saphnelo
В то время как AstraZeneca продвигает Datroway, компания столкнулась с трудностями в продвижении Saphnelo в новой форме. Готовая к рассмотрению заявка на подкожную форму Saphnelo основывалась на промежуточных данных из клинического исследования третьей фазы TULIP-SC, где профиль безопасности был сопоставим с внутривенной формой. Однако к этому времени FDA уже выдало полное ответное письмо, что ставит под угрозу дальнейшие планы компании.
Это обстоятельство подчеркивает сложность операционной среды для фармацевтических компаний, которые стремятся найти новые возможности для одобрения действующих препаратов. Системные проверки и ответные письма FDA могут серьезно повлиять на коммерческие стратегии, что делает необходимость глубокого анализа и обоснования научных данных ключевым элементом для успеха.
В контексте текущих медицинских потребностей и растущего интереса к новым терапиям, такие препараты как Datroway могут значительно изменить подход к лечению определенных типов рака. С учетом будущих исследований и разработок, ожидается, что эти продукты будут оставаться в центре внимания медицинского сообщества и фармацевтической индустрии в целом.